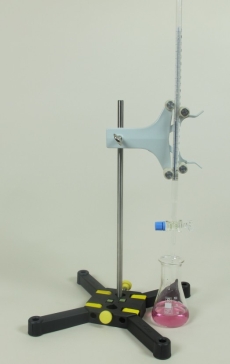
Principio
En este experimento, los alumnos tienen que determinar el valor pKa de una solución de ácido acético con la ayuda de un indicador adecuado (aquí: fenolftaleína). Para ello, se valora un volumen conocido del ácido con un volumen de hidróxido de sodio de concentración conocida (solución patrón) hasta que el indicador cambie de color. El volumen utilizado de la solución patrón se lee en la bureta. La cantidad utilizada se divide por dos. A continuación, se añade la cantidad calculada en forma de ácido acético al recipiente original y se comprueba la solución con una tira de pH. El valor de pH determinado es igual al valor pKa del ácido acético.
Lo que puede aprender sobre
- Cómo calcular el valor pK de los ácidos
Ventajas
- Literatura del experimento disponible para alumnos y profesores: Tiempo de preparación mínimo
- Enseñanza sencilla y aprendizaje eficaz mediante el uso de la literatura de experimentos interactiva disponible