Principio
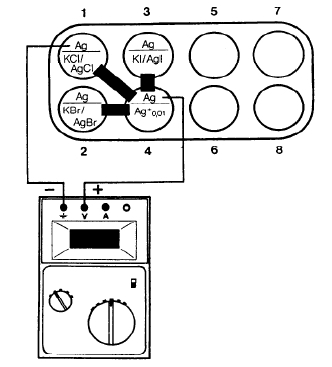
Cuando se añaden unas pocas gotas de una solución muy diluida de nitrato de plata (c =0,01 mol/l) a una solución de 1 molar de haluro de potasio (= KCl, KBr, KI), se produce una precipitación inmediata del haluro de plata correspondiente (AgCl, AgBr, AgI), porque el producto de solubilidad de estas sales sólo muy poco solubles ya se supera incluso con estas pequeñas cantidades de iones de plata añadidas. En estas soluciones de haluros de plata sólo puede quedar libre el número de iones de plata que permite el producto de solubilidad. Como la relación entre la diferencia de concentración y la tensión en una serie de concentración sigue la ecuación de Nernst, el producto de solubilidad, o la concentración de iones de plata, de cada solución de haluro de plata puede calcularse a partir de la tensión medida correspondiente.
Lo que se puede aprender sobre
- Influencia de la solubilidad en el potencial electroquímico
Ventajas
- Enseñanza fácil y aprendizaje eficiente mediante el uso de la experimentación interactiva PHYWE-Software
- El experimento forma parte de un conjunto de soluciones completas con experimentos para el tema de la Electroquímica que se ajusta al plan de estudios internacional: se cubren todos los temas